炭酸水素ナトリウムNaHCO3と炭酸ナトリウムNa2CO3は、名前も化学式も似ていますが、異なる性質を持ちます。
これがややこしくてなかなか覚えにくいですよね。
「なぜ違うのか」それを理解すれば、どっちがどんな性質か、いつでも思い出せるようになるはずです!
それでは、できるだけわかりやすく、優しく解説していきます!
もくじ
性質の違い
炭酸水素ナトリウムと炭酸ナトリウムの主な性質の違いは2つで、
・水への溶けやすさ
・アルカリ性の強さ
です!
そして、炭酸ナトリウムのほうが水に溶けやすく、アルカリ性が強いです!

水への溶けやすさはなぜ違うか
物質が水に溶ける仕組み
そもそも物質が水に溶けるとはどうゆう意味でしょうか。
それは、「物質が水中でばらばらになる(イオンになる)」ということです。(一部例外あり)
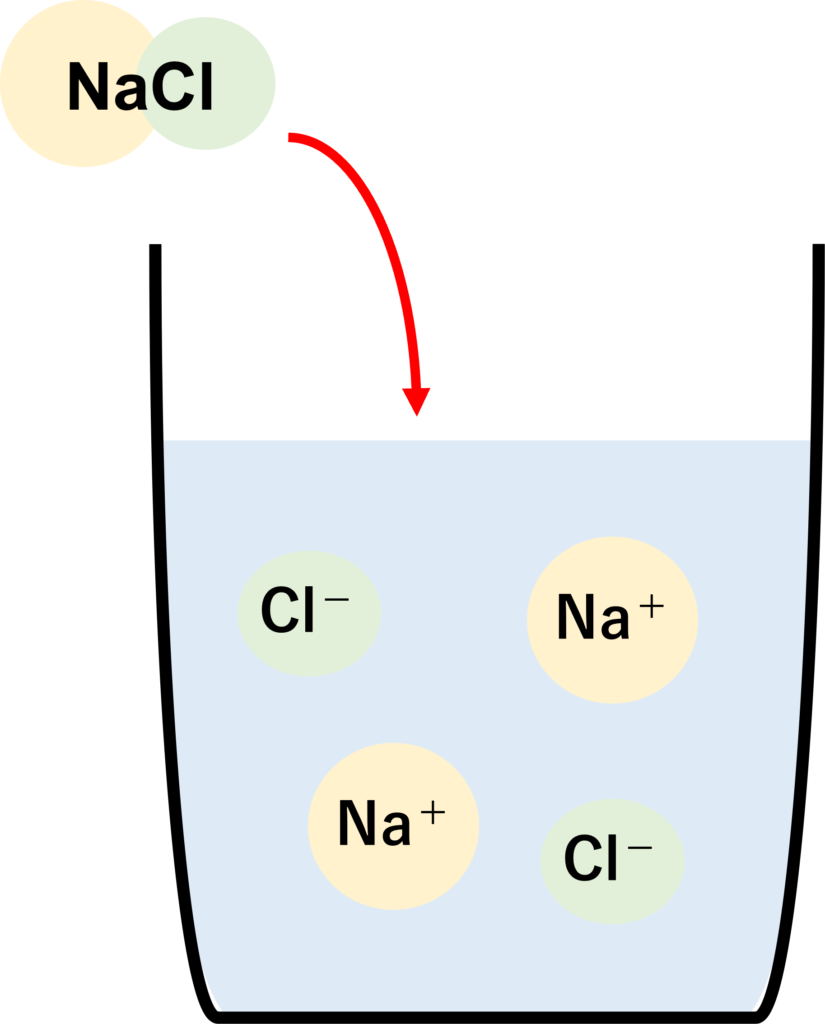
例えば、食塩(NaCl)が水に溶ける時、
NaCl→Na++Cl-
という式で表されるように、NaClはナトリウムイオンと塩化物イオンに分かれ、その結果水に溶けます。
このように物質が水中でイオンに分かれることを「電離」といいます。
物質が水中でイオンに分かれることを電離といい、その結果物質は水に溶ける。
水への溶けやすさ
物質が水中で電離すれば水に溶けた状態になることがわかったと思います。
しかし、すべての物質が水中で完全に電離しているわけではありません。
物質がどの程度電離するかを表した数値を「電離度」といいます。
電離度は0~1の間の値になり、1に近いほど電離しやすいということになります。
この電離度は物質によって様々なので、水に溶けやすい物質があったり、溶けにくい物質があったりします。
物質がどの程度電離するかを表した数値を「電離度」といい、その値は物質によって違うため、水に溶けやすい溶けにくい物質がある。
本題
今までの説明を踏まえると、なぜ炭酸水素ナトリウムと炭酸ナトリウムで水への溶けやすさが違うのか一言で言えます。
それはズバリ、「電離度が違うから」です!
炭酸水素ナトリウムNaHCO3は、
NaHCO3 → Na+ + HCO3-
と電離しますが、このときの電離度は低いです。
一方、炭酸ナトリウムNa2CO3は、
Na2CO3 → 2Na+ + CO32-
と電離し、このときの電離度は高いです。
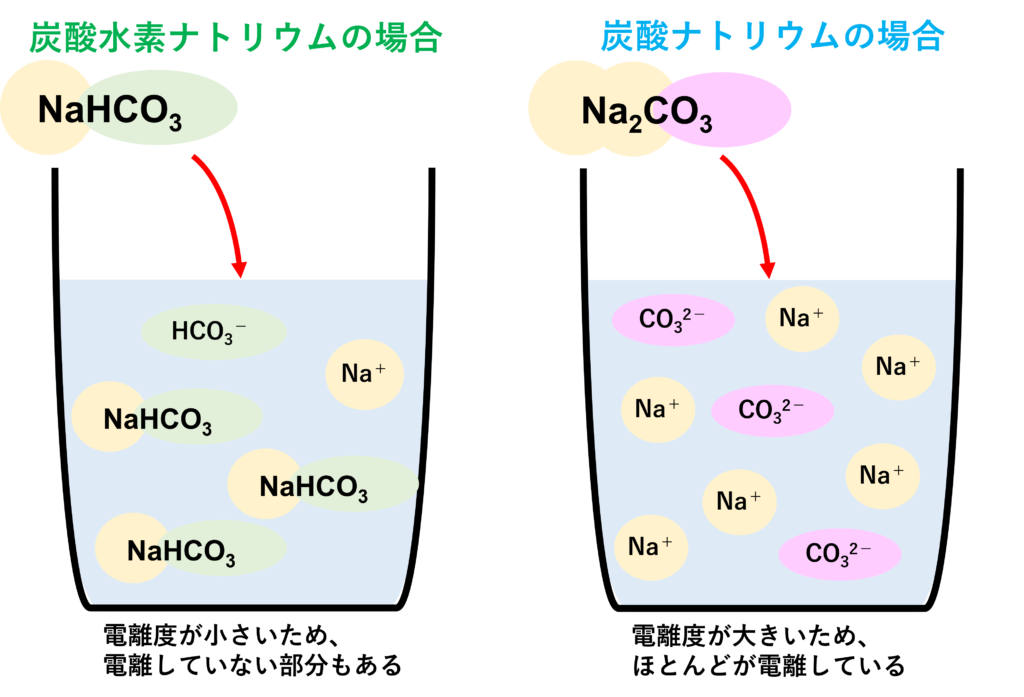
炭酸水素ナトリウムは電離度小
炭酸ナトリウムは電離度大
したがって、炭酸ナトリウムの方が水に溶けやすい
※「ナトリウムはバラバラになりなりやすい、だからナトリウムの数が多い炭酸ナトリウムの方が電離しやすい」と覚えておけば忘れないと思います!
アルカリ性の強さはなぜ違うか
そもそもアルカリ性とは
そもそも酸性・アルカリ性というのは何で決まるのか。
それは水溶液中の水素イオンH+の数と水酸化物イオンOH-の数のどちらが多いかで決まります。
・H+の方が多い→酸性
・H+とOH-が同じ→中性
・OH-の方が多い→アルカリ性
となります。
※実はアルカリ性という言葉は中学までしか使いません。高校では「塩基性」という言葉を使います。知っておきましょう。
炭酸ナトリウムはなぜアルカリ性か
ここからは少し上級編です。
なぜ炭酸ナトリウムはアルカリ性なのかを考えていきましょう。
上述したように、炭酸ナトリウムは水溶液中で、
Na2CO3 → 2Na+ + CO32-
というように電離しています。
あれ?OH-がないですね!ではなぜアルカリ性なのでしょうか。それは、次のような反応が起こるからです。
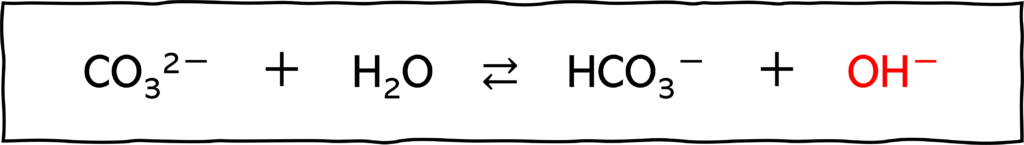
炭酸は、弱酸(=電離度低い)なので、CO32-は水と反応してもとのH2CO3に戻ろうとします。
このとき、OH-が発生するので、炭酸ナトリウムはアルカリ性なのです。
このような現象を「加水分解」といいます。
炭酸ナトリウムの電離によって生じたCO32-が、加水分解を起こして、OH-が生じるから、炭酸ナトリウムはアルカリ性を示す。
炭酸水素ナトリウムはなぜアルカリ性か
では炭酸水素ナトリウムの場合はどうでしょうか。
仕組みは炭酸ナトリウムと同じです。
NaHCO3 → Na+ + HCO3-
電離によって生じたHCO3-が次のように加水分解を起こします。
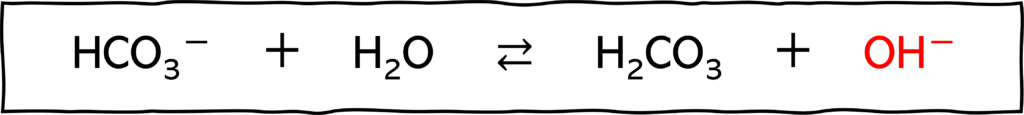
こうしてOH-が生じるためアルカリ性なのです。
炭酸水素ナトリウムの電離によって生じたHCO3-が、加水分解を起こして、OH-が生じるから、炭酸水素ナトリウムはアルカリ性を示す。
本題
さて、では最後に「なぜ炭酸ナトリウムは強いアルカリ性で炭酸水素ナトリウムは弱いアルカリ性なのか」についてです。
ここまでの内容と踏まえると、
・炭酸ナトリウムはCO32-の加水分解
・炭酸水素ナトリウムはHCO3-の加水分解
によってOH-を生じることでアルカリ性になることがわかりました。
理由1
アルカリ性に違いが生じる一つ目の理由は、この2つの加水分解は「起こりやすさ」が違うということです。
CO32-の加水分解は起こりやすく、多くのOH-を生じます。なので炭酸ナトリウムは強いアルカリ性になるのです。
逆にHCO3-の加水分解は起こりにくく、少ししかOH-を生じません。なので炭酸水素ナトリウムは弱いアルカリ性になるのです。

理由2
アルカリ性に違いが生じる一つ目の理由は、そもそも「CO32-の数とHCO3-の数」が違うということです。
そもそも炭酸ナトリウムと炭酸水素ナトリウムは電離度が全然違います。
つまり、水溶液中のCO32-の数とHCO3-の数にも大きな差があるため、当然生じるOH-の数にも大きな差が生じます。
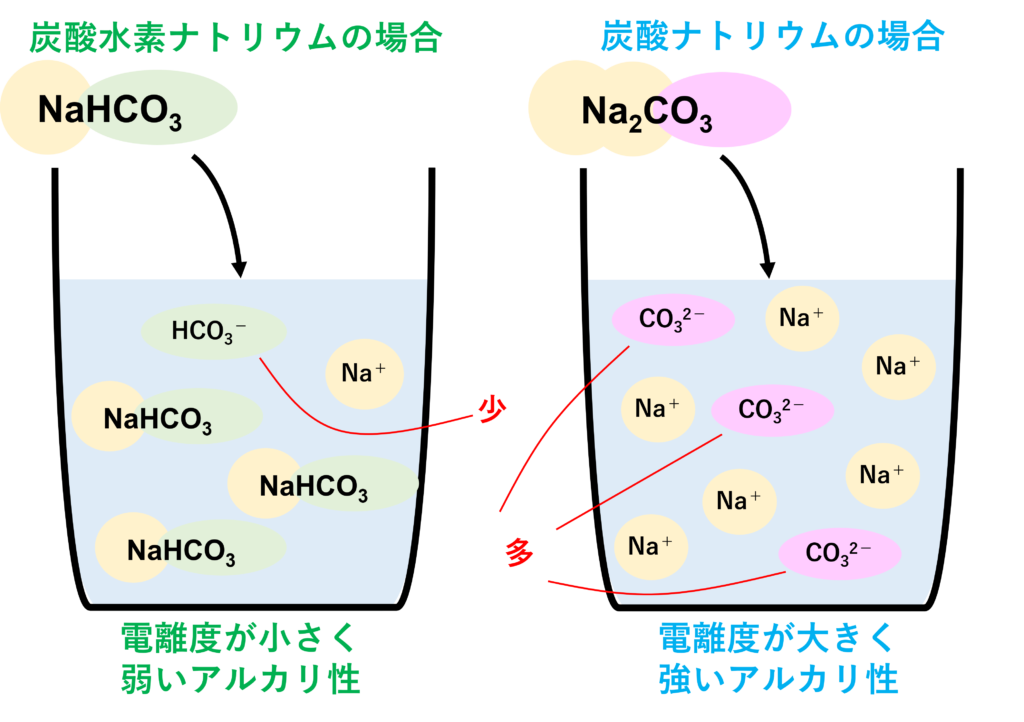
炭酸ナトリウムと炭酸水素ナトリウムのアルカリ性が違う理由!
理由1:CO32-の加水分解は起こりやすく、HCO3-の加水分解は起こりにくいから。
理由2:そもそも電離度の違いから、水溶液中のCO32-の数は多く、HCO3-の数は少ないから。
おまけ:化学式の覚え方
最後におまけで、炭酸水素ナトリウムと炭酸ナトリウムの化学式の覚え方を紹介します!
・炭酸水素ナトリウムは「ナフコさん」
・炭酸ナトリウムは「ナツコさん」
で覚えましょう!